
La corrosión es un proceso electroquímico irreversible en el que un metal reacciona con su entorno para transformarse en productos más estables desde el punto de vista energético, como óxidos, hidróxidos, sulfuros u otros compuestos.
A nivel microscópico, la corrosión metálica se desarrolla a través de celdas electroquímicas locales en la superficie del metal, estableciendo zonas anódicas y catódicas interconectadas por un electrolito.
Ocurre cuando la superficie del metal se deteriora de manera relativamente uniforme. El proceso clásico en metales ferrosos en presencia de agua y oxígeno puede describirse con las siguientes reacciones:
El resultado neto es la formación de hidróxido ferroso, que posteriormente puede transformarse en diversas especies de óxidos e hidróxidos de hierro (herrumbre).
Incluye procesos como picaduras, grietas bajo depósito y corrosión bajo tensión. Estas formas de ataque son especialmente peligrosas porque reducen la sección resistente sin grandes indicios de deterioro superficial, comprometiendo la integridad estructural de componentes críticos.
La corrosión está gobernada por principios termodinámicos y cinéticos:
La galvanización por inmersión en caliente implica inmersión del acero en un baño de zinc fundido (~450 °C). El zinc reacciona metalúrgicamente con el hierro para formar una serie de fases intermetálicas adherentes:
Estas fases forman un recubrimiento complejo con una adherencia metalúrgica excelente y una resistencia química significativa. La capa externa de zinc puro (η) confiere maleabilidad y resistencia a impactos, mientras que las zonas intermetálicas proporcionan dureza y resistencia al desgaste.


Una de las características fundamentales del zinc como recubrimiento protector es su protección catódica activa hacia el acero.
Cuando dos metales distintos o fases con diferentes potenciales estándar están en contacto en presencia de un electrolito, se forma una celda galvánica. El metal con menor potencial electroquímico (más negativo) se comporta como ánodo y se oxida preferentemente, sacrificándose, mientras que el metal más noble actúa como cátodo.
En el sistema zinc‑acero, el zinc tiene un potencial electroquímico más negativo que el hierro. Por tanto:
Este mecanismo describe la base de la protección catódica inherente en recubrimientos galvanizados.
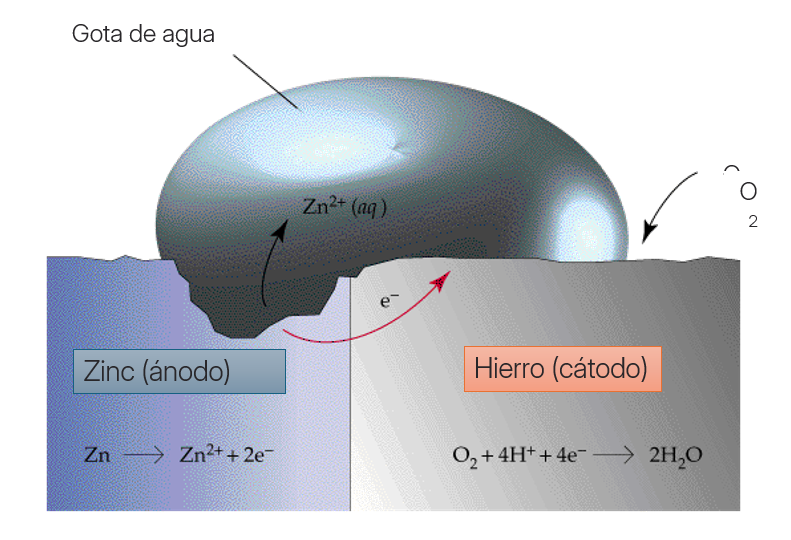
Una de las ventajas críticas del zinc es que incluso cuando el recubrimiento está dañado o presenta roturas, la protección catódica sigue funcionando. En un rasguño donde el acero queda expuesto, el zinc circundante actúa como ánodo de sacrificio, impidiendo la corrosión del acero. Esta capacidad de proteger activamente zonas expuestas sin necesidad de reparación inmediata del recubrimiento es una característica distintiva frente a muchos tratamientos pasivos.